اوربیتال اتمی
|
|||||||
مقدمه
اوربیتال محدودهای از فضای اطراف هسته میباشد که احتمال یافتن الکترون در آن وجود دارد. این احتمال در نزدیکی هسته بیشترین مقدار را دارد. ولی برای تمام نقاطی از فضا که فاصله معینی از هسته دارند، احتمال معینی وجود دارد. هر اوربیتال میتواند حداکثر دو الکترون را در خود جای دهد. دو الکترونی که در یک اوربیتال جای میگیرند، دارای اسپین مخالف هستند.
هر الکترون را میتوان با چهار عدد کوانتومی مشخص کرد که به منزله شناسنامه الکترون هستند و فاصله نسبی الکترون از هسته (n) ، لایه فرعی و شکل اوربیتال (L) ، جهت گیری اوربیتال در فضا (s) را بیان میکنند. بر اساس اصل طرد پاولی در یک اتم هیچ دو الکترونی را نمیتوان یافت که تمام چهار عدد کوانتومی آنها یکسان باشد.
تاریخچه
در مورد ساختمان اتم و نحوه قرار گرفتن الکترونها و پروتونها در آن بررسیهای زیادی توسط دانشمندان انجام شده و نظریههای مختلفی ارائه شده است. تامسون اتم را به شکل کرهای یکنواخت از بارهای مثبت تا شعاع 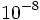 تصور میکرد که بارهای منفی در محیط خارجی کره پراکندهاند. رادرفورد در سال 1911 با استفاده از ذرات آلفا دلایل قانع کنندهای مبنی بر وجود هسته اتم ارائه داد. او اتم را بصورت کره ای تصور میکرد که هسته در وسط آن قرار دارد و الکترونها به فواصل نسبی بینهایت زیاد در خارج از هسته قرار دارند. نیلز بوهر در سال 1913 نظریه ساختمان الکترونی اتم را پیشنهاد کرد.
تصور میکرد که بارهای منفی در محیط خارجی کره پراکندهاند. رادرفورد در سال 1911 با استفاده از ذرات آلفا دلایل قانع کنندهای مبنی بر وجود هسته اتم ارائه داد. او اتم را بصورت کره ای تصور میکرد که هسته در وسط آن قرار دارد و الکترونها به فواصل نسبی بینهایت زیاد در خارج از هسته قرار دارند. نیلز بوهر در سال 1913 نظریه ساختمان الکترونی اتم را پیشنهاد کرد.
این نظریه بر اساس مدل اتمی رادرفورد ، نظریه کوانتومی پلانک و دادههای تجربی حاصل از مطالعه طیفهای اتمی قرار داشت، و بیان میکرد که الکترون اتم هیدروژن فقط میتواند در مدارهای کروی معین (مدارها یا ترازهای انرژی) که بطور متحدالمرکز دور هسته قرار دارند، وجود داشته باشد. این مدارها تابع محدودیت کوانتومی است. شرودینگر در سال 1926 با طرح معادلهای که در آن محدودیت کوانتومی انرژی الکترون و تصور الکترون بصورت موج ساکن ، با هم تلفیق شده بود، تابع موجی الکترون (ψ) را معرفی کرد که مختصات مکان الکترون در فضایی که الکترون در آن یافت میشود و انرژی الکترون از لحاظ ریاضی را به هم مربوط کرد.
اگر الکترون را بصورت ذرهای در حال حرکت به دور هسته در نظر بگیریم، ψ2 متناسب با احتمال یافتن الکترون در جزو معینی از فضاست و احتمال یافتن الکترون در ناحیهای که ابر الکترونی غلیظتر باشد بیشتر است.
 |
تفسیر مکانیکی اوربیتال
شدت هر موج با مجذور دامنه آن متناسب است. تابع موجی (ψ) ، تابع دامنه است. مجذور دامنه یا مجذور تابع موجی برای یک حجم کوچک در هر موقعیتی از فضا با چگالی بار الکترونی در آن حجم متناسب است. میتوان تصور کرد که بار الکترونی به سبب حرکت سریع الکترون بصورت ابر باردار در فضای دور هسته گسترده شده است. این ابر در برخی نواحی غلیظتر از برخی نواحی دیگر است.
احتمال یافتن الکترون در هر ناحیه معین متناسب با چگالی ابر الکترونی در آن ناحیه است. این احتمال در ناحیهای که ابر الکترونی غلیظتر باشد، بیشتر خواهد بود. این تفسیر کوششی برای توصیف مسیر الکترون به عمل نمیآورد، بلکه فقط پیشبینی میکند که احتمال یافتن الکترون در کجا بیشتر است.
از نظر مکانیک کوانتومی هیچ محدودیتی برای وجود الکترون در فضا اطراف هسته وجود ندارد. پس بینهایت اوربیتال وجود دارد.
اعداد کوانتومی
مکانیک موجی که نظریه شرودینگر اساس آن میباشد با استفاده از چهار عدد کوانتومی وضعیت الکترون را توصیف میکند. این اعداد عبارتند از :
عدد کوانتومی اصلی
این عدد نشاندهنده ترازهای انرژی است که الکترونها در آن ترازها به دور هسته گردش میکنند و عدد صحیحی میباشد. این عدد میتواند کلیه مقادیر اعداد صحیح مثبت به استثنای صفر را قبول کند.
عدد کوانتومی اندازه حرکت زاویهای مداری
آرنولد زمر فیلد در سال 1916 پیشنهاد کرد که هر مدار بوهر (n) با شرط n>1 از لایههایی فرعی با اختلاف انرژی کم تشکیل شدهاست. به هر لایه فرعی یک عدد کوانتومی (L) نسبت داده میشود. این عدد نشان دهنده شکل هندسی توزیع تابع احتمال پیدا کردن الکترون در فضای اطراف هسته میباشد وکلیه مقادیر L=0,1,2, … , n-1 را اختیار کند.
عدد کوانتومی مغناطیسی مداری
تعداد اوربیتالهای یک تراز فرعی را میتوان از این عدد استنتاج کرد که در اثر میدان مغناطیسی هر تراز L به این ترازها شکافته میشود. بعنوان مثال میدان مغناطیسی بر اوربیتال کروی S که با عدد L=0 مشخص میشود، تاثیری ندارد چون S تقارن کروی دارد و در تمام جهتها بطور یکسان تحت تاثیر خطوط نیرو قرار میگیرد. این عدد که با m نشان داده می شود، مقادیر ممکن این عدد عبارتند از :
عدد کوانتومی مغناطیسی اسپینی
این عدد مشخص کننده حرکت تقدیمی الکترون است و با  نشان داده میشود و میتواند مقادیر 2/1+ , 2/1- را اختیار کند.
نشان داده میشود و میتواند مقادیر 2/1+ , 2/1- را اختیار کند.
ابر الکترونی و مکان الکترون
در مورد یک الکترون در حالت n=1 هیدروژن ، ابر باردار بالاترین چگالی را در نزدیکی هسته دارد و بتدریج که فاصله از هسته افزایش مییابد، رقیقتر میشود. احتمال یافتن الکترون در حجم کوچکی از فضا ، در نزدیکی هسته ، بیشترین مقدار را دارد و با افزایش فاصله از هسته به سمت صفر میل میکند.
لایههای کروی بسیار نازکی را که یکی پس از دیگری بطور متحدالمرکز به دور هسته قرار دارند، تصور کنید. احتمال یافتن الکترون در واحد حجم فضای نزدیک به هسته بیشترین مقدار خود را دارد. ولی در عوض یک لایه نزدیک به هسته ، در مقایسه با لایههای دورتر ، تعداد کمتری واحد حجم را در بر میگیرد. احتمال شعاعی هر دو این عوامل را با هم به حساب میآورد.
نمودار سطح مرزی
احتمال یافتن الکترون در تمام نقاطی که از هسته به فاصله  برابر مقداری است که از طریق نظریه بور برای شعاع لایه n=1 تعیین شده است. در نظریه بوهر ،
برابر مقداری است که از طریق نظریه بور برای شعاع لایه n=1 تعیین شده است. در نظریه بوهر ،  فاصلهای است که همواره الکترون لایه n=1 از هسته دارا است. در مکانیک موجی
فاصلهای است که همواره الکترون لایه n=1 از هسته دارا است. در مکانیک موجی  فاصلهای از هسته است که الکترون در آن حضور بیشتری دارد.
فاصلهای از هسته است که الکترون در آن حضور بیشتری دارد.
از آنجا که اصولا در هر فاصله معین از هسته ، الکترون امکان حضور دارد، ترسیم ناحیهای با مرز مشخص که احتمال 100 درصد وجود الکترون را در بر بگیرد، ناممکن است. اما میتوان سطح مرزی را ترسیم کرد که بتواند نقاط با احتمال یکسان را به هم بپیوندد و در برگیرنده حجمی باشد که در آن ، احتمال یافتن الکترون زیاد و مثلا در حدود 90 درصد است. چنین شکلی که نمودار سطح مرزی نامیده میشود، برای الکترون اتم هیدروژن در حالت n=1 بصورت کروی میباشد.
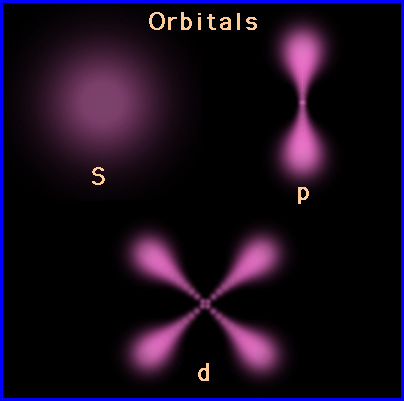
انواع اوربیتال
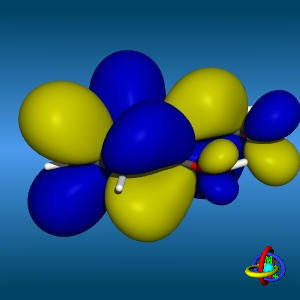
اوربیتال S
اوربیتالهای S دارای تقارن کروی میباشد، تراز n=1 حداکثر دارای دو الکترون است. بنابراین تراز فرعی 1S و 2S و 3S و... هم تقارن کروی دارند، با این تفاوت که اندازه آنها بزرگتر از اوربیتال 1S میباشد.
اوربیتال p
اوربیتال p از سه اوربیتال فرعی تشکیل شده است. هر اوربیتال p به شکل دو کره تغییر شکل یافته است که میتوان آنها را در امتداد یکی از محورهای سه گانه مختصات (z,y,x) تصور کرد از این رو اوربیتالهای p را با  مشخص میکنند که در سه جهت مختلف قرار گرفتهاند. اوربیتالهای p از لحاظ انرژی برابرند و در غیاب میدان مغناطیسی نمیتوان تفاوتی بین الکترونهایی که این اوربیتالها را اشغال کردهاند قایل شد. ولی در بررسیهای طیفی که تحت تاثیر یک میدان مغناطیسی قرار میگیرند، هر اوربیتال p به سه خط شکافته میشوند.
مشخص میکنند که در سه جهت مختلف قرار گرفتهاند. اوربیتالهای p از لحاظ انرژی برابرند و در غیاب میدان مغناطیسی نمیتوان تفاوتی بین الکترونهایی که این اوربیتالها را اشغال کردهاند قایل شد. ولی در بررسیهای طیفی که تحت تاثیر یک میدان مغناطیسی قرار میگیرند، هر اوربیتال p به سه خط شکافته میشوند.
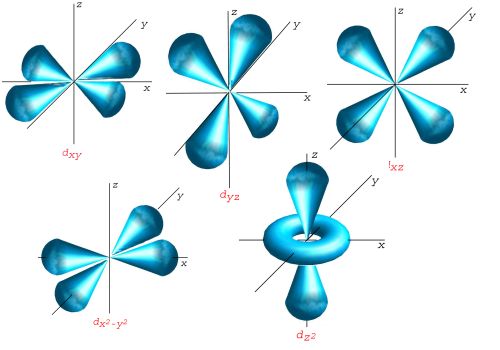 |
اوربیتال d
اوربیتالهای d از 5 اوربیتال فرعی تشکیل شدهاند که جهت گیریهای متفاوتی در فضا دارند ولی از لحاظ انرژی باهم همارز هستند. این اوربیتالها عبارتند از:

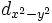
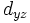
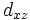

|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
درجه انحطاط
تعداد الکترونهایی که مقدار انرژی برابر داشته باشند، درجه انحطاط یا چندگانگی نامیده میشوند. حداکثر تعداد الکترونهای هر تراز از فرمول 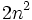 بدست میآیند.
بدست میآیند.

